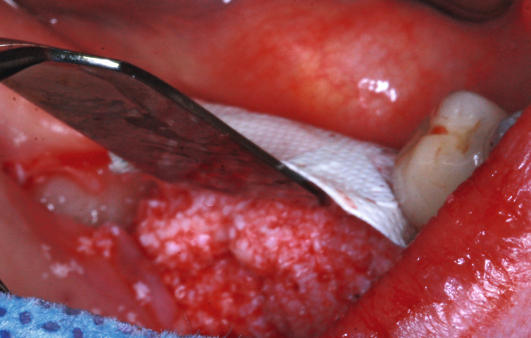
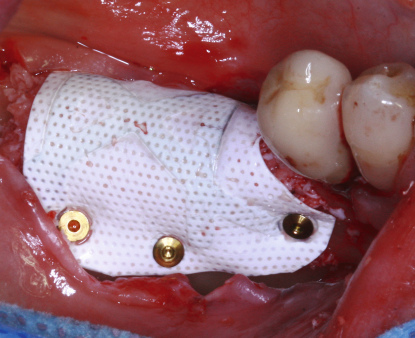
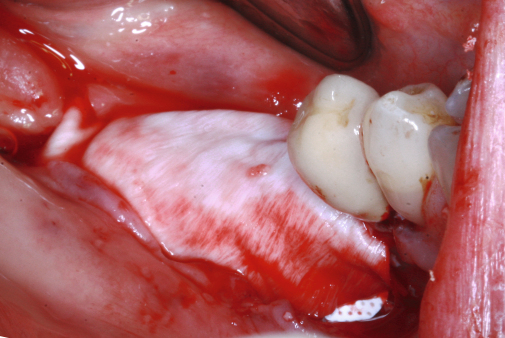
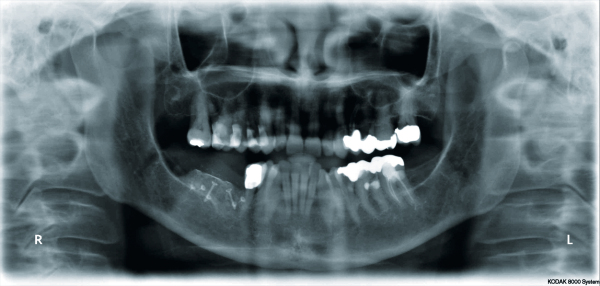
GTR/GBR-Prinzip: Wann welche Membranen?
Membranen werden schon seit vielen Jahren in der gesteuerten Geweberegeneration (Guided Tissue Regeneration, GTR) und gesteuerten Knochenregeneration (Guided Bone Regeneration, GBR) angewendet. Das GTR/GBR-Prinzip beruht auf der Platzierung einer Barrieremembran, um langsam proliferierende regenerative Zelltypen wie Osteoblasten und parodontale Zellen von schnell proliferierenden Epithel- und Bindegewebszellen zu trennen und somit eine voraussagbare Regeneration verloren gegangenen Gewebes zu schaffen. Resorbierbare Kollagenmembranen mit verlängerten Standzeiten scheinen bei einigen Indikationen Vorteile zu haben.
Die erste Generation von Barrieremembranen bestand aus nichtresorbierbaren Materialien wie expandiertem Polytetrafluorethylen (ePTFE) und Celluloseacetat oder Titan. Bitte nennen Sie die Vor- und Nachteile dieser Varianten. Wann sind sie indiziert, wann kontraindiziert?
Wessing: Die Antwort liegt im Prinzip der GTR/GBR, also der Hohlraumschaffung, der Hohlraumabschirmung und den damit verbundenen Anforderungen an Membranen für diese Technik. Zu den wichtigsten Parametern gehören Biokompatibilität, Gewebeintegration, Zellokklusivität, Nährstofftransfer, Raumschaffung und -erhalt sowie das Handling [1].
Die Vorteile der nichtresorbierbaren e-PTFE-Membranen, vor allem der titanverstärkten, liegen in der guten Raumschaffung und dem langfristigen Raumerhalt über den gesamten Zeitraum bis zur Eröffnungsoperation.
Was sind die Hauptindikationen?
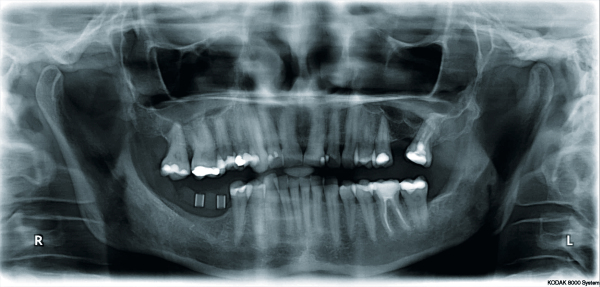
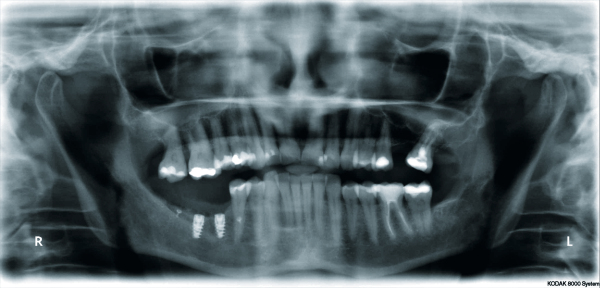
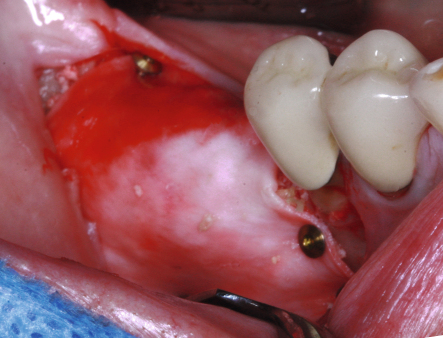
Wessing: Die Hauptindikation für die e-PTFE-Membranen sehe ich im Bereich der GBR zur Behandlung kritischer Defekte, insbesondere der nicht raumschaffenden ein-, zweiwandigen Defekte nach Misch & Dietsh [2] und der größeren Defekte der HVC-Klassifizierung nach Wang, horizontal ab 6 mm und/oder vertikal ab 3 mm. Hier möchte ich vor allem den vertikalen Kieferkammaufbau im posterioren Unterkiefer nennen [3].
Welche Nachteile gibt es?
Wessing: Die Nachteile liegen in der geringeren Biokompatibilität und Gewebeintegration. So kommt es beim Einsatz von e-PTFE-Membranen signifikant häufiger zu frühzeitigen Membranexpositionen und folglich zu einer verminderten Knochenregeneration. Und: Es braucht eine größere Eröffnungsoperation, um die Membran zu entfernen.
Eine Alternative sind resorbierbare Membranen …
Wessing: Korrekt, kommerziell erhältlich sind sie erstaunlicherweise bereits seit 1982. Untersucht wurden die ersten resorbierbaren Membranen ebenso wie die nichtresorbierbaren PTFE-Membranen zunächst für die GTR. Blumenthal publizierte 1990 erstmals die Verwendung einer chemisch vernetzten bovinen Kollagenmembran, (Periogen, Collagen Corporation, Palo Alto, USA) zur Behandlung von Parodontaldefekten am Menschen [4]. Anfang der 90er Jahre wurde vor allem an der Entwicklung und klinischen Erforschung von resorbierbaren Membranen aus Polylactiden, Polyglycoliden, Copolymeren sowie chemisch vernetzten Kollagenmembranen gearbeitet.
Wann haben sich die resorbierbaren Varianten wirklich etabliert?
Wessing: Vor rund 15 bis 20 Jahren. Erst die Entwicklung und systematische Untersuchung von nativen Kollagenmembranen Mitte bis Ende der 1990er Jahre mit guten Ergebnissen in der Knochenregeneration bei niedrigen Komplika‧tionsraten haben dazu geführt, dass sich die resorbierbaren Kollagenmembranen nicht nur als Alternative durchgesetzt, sondern die nichtresorbierbaren in vielen Ländern tatsächlich abgelöst haben. Es gibt allerdings Unterschiede in puncto Herkunft, Kollagentyp und Vernetzungsgrad.
Wie lange „halten“ resorbierbare Kollagenmembranen im Durchschnitt?
Wessing: Die durchschnittliche Standzeit kann man pauschal nicht benennen. Je nach Vernetzungsgrad und Herkunft weisen sie andere Eigenschaften auf: Einige werden bereits nach wenigen Wochen resorbiert, andere, zum Beispiel chemisch vernetzte, können die Barrierefunktion sechs Monate lang aufrechterhalten. Ein Expertenmeeting renommierter Fachleute im Jahr 2008 – Geistlich Scientific Roundtable on Membranes, Luzern – kam zu dem Schluss, dass der kritische Zeitpunkt für die Zellokklusivität bei zwei bis vier Wochen liegt. Allerdings spielen bei GBR und auch GTR noch weitere Faktoren eine große Rolle, insbesondere die Größe des zu regenerierenden Bereichs, die Defekttopografie und das verwendete Augmentationsmaterial. Bei großen Augmentationen – zum Beispiel mit der in unserer Praxis favorisierten „Sausage Technique“ nach Urban – möchte ich eine möglichst lange mechanische Stabilisierung der partikulären Augmentationsmaterialien gesichert wissen.
Die benötigte Barrieredauer ist also abhängig vom Defekt?
Wessing: Korrekt, so sieht es übrigens auch die bereits zitierte Expertengruppe.
Nobel Biocare wirbt für die resorbierbare Kollagenmembran creos xenoprotect mit Standzeiten von zwölf bis 16 Wochen. Wie wirkt sich die längere Standzeit bei Ihren Fällen aus?
Wessing: Positiv, die Ergebnisse beispielsweise bei offener Einheilung (Socket Preservation), großvolumigen Aufbauten oder bei frühzeitiger Membranexposition scheinen hinsichtlich der Knochenaufbaurate den zuvor von uns verwendeten Membranen deutlich überlegen zu sein. Die längere Standzeit wurde bei der creos xenoprotect nicht durch eine chemische Vernetzung erreicht, sondern durch ein faseriges Netzwerk porkiner Kollagen- und Elastinfasern. Somit entfallen auch die bekannten Probleme der chemischen Quervernetzung wie zum Beispiel höhere Membranexpositionsraten.
Wann reicht creos xenoprotect allein nicht aus? Wann verwenden Sie zusätzlich Knochenersatzmaterial?
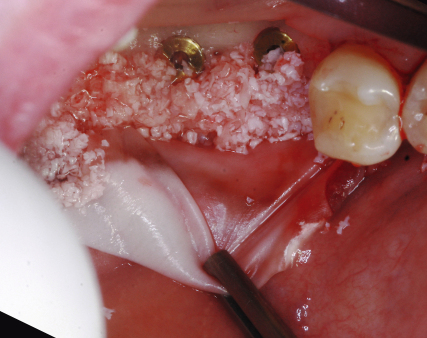
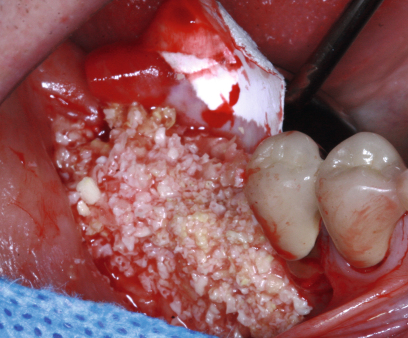
Wessing: Wir kombinieren grundsätzlich immer mit „Füllern“, also autologem Knochen oder Knochenersatzmaterial. Die GBR-Technik ist dann signifikant erfolgreicher [5]. Bei raumschaffenden Defekten, etwa bei fehlender bukkaler Lamelle und auch bei rein horizontalen Defekten, ist die GBR mittels resorbierbarer Kollagenmembranen in Verbindung mit den angesprochenen „Füllern“ eine zuverlässige und reproduzierbare Behandlungsform. Erste publizierte Ergebnisse – noch keine evidenzbasierten Daten – der vergangenen Jahre scheinen mit speziellen Techniken zwar auch den vertikalen Knochenaufbau möglich zu machen, aber meiner Meinung nach ist es noch zu früh, um dazu genauere Aussagen zu treffen.
Wann muss es doch die nichtresorbierbare Membran sein?
Wessing: Prinzipiell können alle raumschaffenden Defekte mit Kollagenmembranen behandelt werden. Problematisch wird es bei nicht raumschaffenden Defekten von mehr als 6 mm horizontal, dem vertikalen Aufbau von mehr als 3 mm und bei der Verwendung von mechanisch instabilem Augmentationsmaterial, zum Beispiel rein autologen Knochenchips. Dann setzen auch wir nichtresorbierbare Membranen ein. Werden große, auch rein horizontale Defekte mittels GBR ohne die Verwendung von fixierten Knochenblöcken oder langsam resorbierbaren Knochenersatzmaterialen angestrebt, sollten ebenfalls nichtresorbierbare Membranen verwendet werden. Denn in diesen Fällen muss die Raumerhaltung durch die eigene Formstabiliät der Membran erreicht werden, weil Knochenaufbauten mit rein autologen Knochenchips (Knochenmühle oder Safe‧scraper) nicht dauerhaft stabil sind und deutlich schneller resorbiert werden als zum Beispiel eine Mischung daraus mit langsam resorbierbaren Knochenersatzmaterialien.
Kommen wir zur Fixierung. Wie gehen Sie in Ihrer Praxis vor?
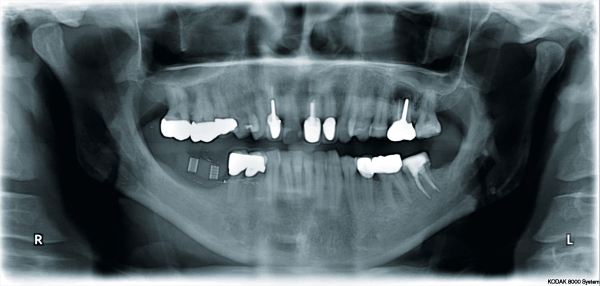
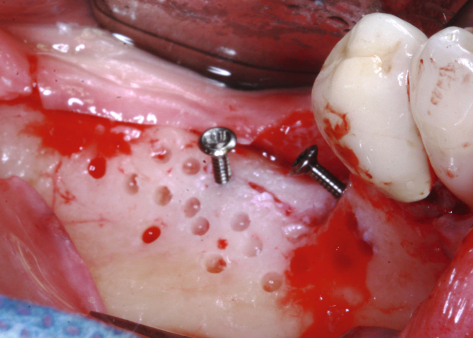
Wessing: Es gibt bis heute noch keine evidenzbasierten Daten für den Vorteil einer Membranfixierung. Eigene Beobachtungen sowie einige wenige Studien zu diesem Thema sprechen jedoch dafür. Bei Fixierung der Membran in Kombination mit partikulären Augmentationsmaterialien scheint die Expositionsrate geringer und der Knochenzuwachs höher zu sein. Eine aktuelle Kadaverstudie aus diesem Jahr konnte zeigen, dass bei fehlender Membranfixierung durch Manipulation des Lappens beim Vernähen eine Migra‧tion der Knochenaufbaupartikel ins umliegende Gewebe stattfindet [6]. Bei der Verwendung von fixierten Knochenblöcken in Verbindung mit Kollagenmembranen scheint die Membranfixierung dagegen eine untergeordnete Rolle zu spielen.
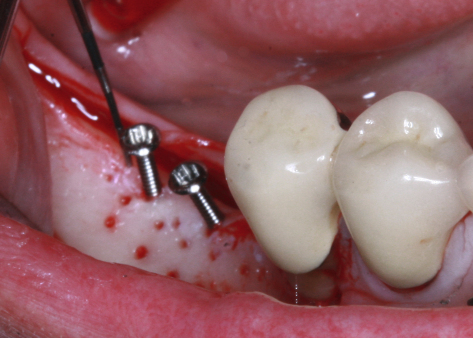
Welche Pins favorisieren Sie?
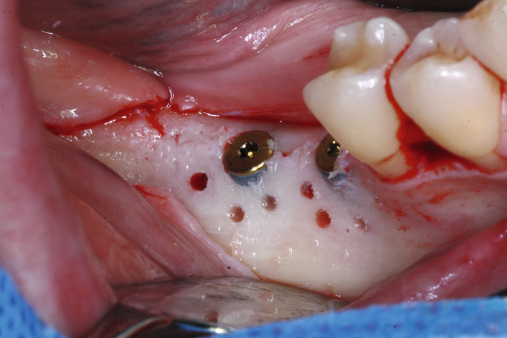
Wessing: Titanpins; sie sind stabil genug und lassen sich auch ohne Vorbohrung in dicken, kortikalen Knochen einbringen. Um sie zu entfernen, muss auch nicht immer eine große Eröffnungsoperation durchgeführt werden. Häufig lassen sich die Pins nach einiger Zeit (sechs bis acht Wochen) durch die Schleimhaut mit dem Finger ertasten und leicht entfernen, ein Zwei- bis Drei-Millimeter-Schnitt über dem Pin mit nachfolgender Einzelknopfnaht – das war’s. Ganz wichtig: Sie sollten exakt im rechten Winkel auf den darunterliegenden Knochen aufgesetzt und eingebracht werden. Dabei muss der Behandler penibel darauf achten, den n. mentalis, den n. alveolaris inferior oder die Wurzeln der Nachbarzähne nicht zu verletzen.
Welche Studien belegen den Erfolg resorbierbarer Membranen, speziell der neuen creos xenoprotect?
Wessing: Kollagenmembranen sind in den vergangenen 15 Jahren intensiv untersucht und dokumentiert worden. Daher beschränke ich mich auf Studien zur creos xenoprotect. Die Grundvoraussetzungen für eine gute Membran – Biokompatibilität, Gewebeintegration und schnelle Revaskularisierung – wurden von Bozkurt et al. im Tierversuch erforscht und 2014 im Clinical Oral Implants Research veröffentlicht [7]. Wir haben auf der EAO 2013 in Dublin in einem Poster Untersuchungen zur Reißfestigkeit und auch zur Nahtausreißfestigkeit der Membran präsentiert. Sie ist in diesem Punkt sämtlichen getesteten Referenzprodukten überlegen, selbst einer PTFE-Membran. Die absoluten Werte sind im Supplement-Band der Clinical Oral Implants Research zum Kongress 2013 veröffentlicht [8]. Arrighi et al. haben 2014 auf dem Kongress der International Association for Dental Research in Kapstadt eine etwa halb so große Expansion nach Rehydratation verglichen mit einem bekannten Referenzprodukt [9]. Die erste klinische Untersuchung zu horizontalen Knochenaufbauten mittels GBR plus creos xenoprotect unserer Praxis wurde 2014 im International Journal of Periodontics and Restorative Dentistry zur Veröffentlichung angenommen. Verglichen mit der rezenten Literatur zeigte sie eine vergleichsweise geringe Dehiszenzrate von nur zwölf Prozent [10].
Ihr Fazit?
Wessing: Ausreichend hohe mechanische Eigenschaften einer resorbierbaren Kollagenmembran im Hinblick auf die Fixierung und Zugfestigkeit vereinfachen umfassende Knochenaufbauten mittels GBR. Denn die partikulären Ersatzmaterialien lassen sich durch die Membran sicher an Ort und Stelle fixieren. (ab)
Dr. Bastian Wessing
ist Partner und stellv. Leiter der Praxisklinik Aachen. Zu seinen Behandlungsschwerpunkten zählen Implantologie, Prothetik und komplexe Rehabilitationen.
info@praxisklinikaachen.de