Implantatoberflächen: Die Mischung macht’s
Die Bearbeitung der Implantatoberfläche gilt als wichtiges Kriterium für eine sichere Knochen- und Weichgewebsanlagerung an das Implantat. Die richtige Mischung aus Rauigkeit und Topografie der Implantatoberfläche ist vor allem für die Sekundärstabilität entscheidend. Für die Oberflächenstrukturierung stehen verschiedene Techniken zur Verfügung. Das Spektrum reicht von additiven Verfahren (Titanplasmabeschichtung, Hydroxylapatit) über subtraktive Techniken (Sandstrahlung, Ätzung, spezielle Laserbehandlung) bis hin zu mikrostrukturierten Oberflächen. Fachleute führender Hersteller sagen, worauf es ankommt.
Aktuell wird viel über die Implantatoberflächen diskutiert, auf welches Verfahren setzen Sie?
Biehl: Für uns als Pionier in der Oberflächentechnologie ist das Strahlen mit anschließendem Ätzen Stand der Technik. Diese Bearbeitung führt zu einer mikrorauen Oberfläche, die – im Vergleich zu einer maschinierten – eine deutlich vergrößerte Anlagerungsfläche besitzt. Das zeigt sich etwa bei der FRIADENT plus Oberfläche, deren Benetzungseigenschaften für die initiale Phase der Knochenheilung maßgeschneidert sind. Denn die primäre Zellanhaftung auf der Mikrostruktur der Oberfläche wird aktiviert. Genauso wie bei der mikrorauen OsseoSpeed Oberfläche – beide haben sich in allen Indikationen und Belastungsformen klinisch bewährt.
Große Holthaus: Auch unserer Erfahrung nach sind die gestrahlt-geätzten Implantatoberflächen sehr gut universell einsetzbar. Doch unabhängig von der Art der Bearbeitung kommt es auch auf die Reinheit der Implantatoberfläche an. Rückstände der Fertigungsprozesse, beispielsweise Strahlmittel oder Säure – das darf nicht sein.
Was heißt das konkret?
Große Holthaus: Die Literatur belegt, dass eine homogen verteilte und verlässlich reproduzierbare Flächenrauigkeit der Implantatoberfläche mit dem Normrauheitsparameter Sa = 1–2 µm sich hierbei bewährte. Unsere Implantate bestehen aus reinem Titan, sogenanntem commercially pure Titan (cp Ti).
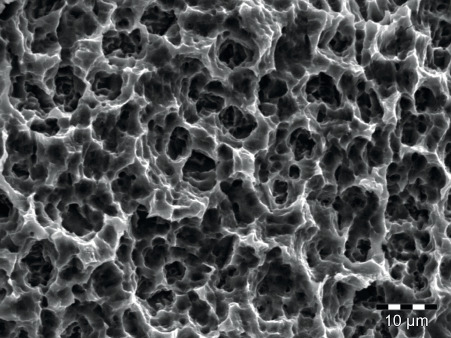
- Die Implantatoberfläche TiPurePlus wird zum einen mit reinem Keramikstrahlmittel konditioniert, wodurch die Oberfläche angeraut wird. Damit erreicht man eine gezielte und homogene, also gleichmäßig verteilte Flächenrauigkeit. (Abb. 12).
- Zum anderen werden die Implantate mit hochreiner Säure geätzt, um eine reproduzierbare Topografie mit gezielter Oberflächenrauigkeit zu erzielen. Typisch für die TiPurePlus Oberfläche sind gleichmäßig verteilte Ätzwaben und -grübchen, die eine gute Osseointegration ermöglichen (Abb. 13, 14). Dabei werden zudem Restanteile des Strahlmittels aus der Oberfläche herausgelöst, so dass unsere Implantate eine Reinheit von mehr als 98 Prozent Titan an der Oberfläche aufweisen. Sowohl Teile des Gewindes als auch die Spankammern sind gleichermaßen rein. Diese reproduzierbare Fertigung der Oberfläche ermöglicht eine gute Osseointegration während der Einheilphase.
Auch Straumann setzt auf Ätzen und Strahlen statt auf Beschichten, warum?
Appert: Jede Beschichtung weist eine zusätzliche Schwachstelle an der Grenzfläche auf. Wir bieten deshalb zwei Varianten rauer Oberflächen an:
- Bei der SLA Oberfläche wird durch eine grobe Sandstrahlung eine Makrorauheit auf der Titanoberfläche generiert. Darauf folgt eine Säureätzung, die eine Mikrorauheit erzeugt.
- Die SLActive Oberfläche wird ebenfalls standgestrahlt und mit Säure geätzt. Allerdings wird die Aufarbeitung unter Schutzgas vorgenommen und das Implantat in Flüssigkeit gelagert. Diese neue Oberflächengeneration zeichnet sich durch eine chemisch aktive und hydrophile Oberfläche aus.
Für SLA Implantate gibt es Zehnjahresdaten mit exzellenten Erfolgs- und Überlebensraten, für SLActive Fünfjahresdaten.
Anodische Oxidation, Titanoxid, das sind Ihre Stichworte, Herr Dr. Holst?
Holst: Richtig, Nobel Biocare favorisiert das den additiven Verfahren zuzurechnende TiUnite, ein Titanoxid, das sich mittels Anodisierung durch Funkenentladung in einem P-haltigen Elektrolyt zu einem osseokonduktiven keramischen Biomaterial als poröse Oberfläche mittlerer Rauigkeit entwickelt. Die klinische Wirksamkeit und Sicherheit wurde bisher in über 250 wissenschaftlichen Publikationen mit mehr als 35.000 Implantaten und 11.000 Patienten in allen Indikationen und Belastungsprotokollen belegt. Zudem sind mehr als 700 internationale peer-reviewed Publikationen zu unserer Oberfläche veröffentlicht worden.
Seit wann gibt es diese porösen Oberflächen?
Holst: Seit 2000 wird die TiUnite Oberfläche verwendet und seither in klinischen Studien dokumentiert. Neben einer Vielzahl von Studien, die den erfolgreichen klinschen Einsatz über fünf Jahre und mehr dokumentieren, beträgt das längste klinisch kontrollierte Follow-up elf Jahre. Die Überlebensraten sind mit bis zu 100 Prozent hoch, und der marginale Knochen verbleibt nach einer initialen Umbauphase stabil.
Sie favorisieren eine zusätzliche Beschichtung, Frau Strauß?
Strauß: Ja, BIOMET 3i bevorzugt die Kombination Abstrahlen, Säureätzung und Nano-Beschichtung mit Hydroxylapatit, denn hiermit rauen wir die Implantatoberfläche in drei verschiedenen Stufen auf. Unsere Oberfläche war übrigens 1996 die erste aufgeraute Implantatoberfläche auf dem Markt, die mit einer subtraktiven Methode, also der doppelten Säureätzung, erzielt wurde. Diese Oberfläche bietet eine Rauigkeit im feinen Mikrometerbereich, zwischen 1 und 3 µm.
Warum die maschinierte Schulter? War das Periimplantatitisrisiko 1996 bereits ein Thema?
Strauß: Wir haben uns schon damals damit befasst. Unsere Osseotite Implantate verfügten bereits vor fast 20 Jahren über ein Hybriddesign, also einen rauen säuregeätzten Implantatkörper mit einer maschinierten Schulter. Das Ziel: Minimierung des Risikos für Periimplantitis. So bekamen die Implantate bereits damals eine FDA-Zulassung für das Verfahren der Frühbelastung (zwei Monate Einheilungszeit).
Was hat es mit der neuen Nanobeschichtung auf sich?
Strauß: Die Oberfläche unseres NanoTite Implantats entstand 2007 durch das gesonderte Aufbringen von Nanokristallen des Hydroxylapatits auf die Osseotite Implantatoberfläche. Durch diesen Prozess der Einzelkristallauflagerung ermöglicht die NanoTite-Implantat-Oberfläche eine Verbesserung der Osseointegration in der frühen Einheilphase, kurz Bone Bonding, also die Verzahnung der Verbindung von Knochenmatrix mit der Oberfläche des Implantats. Im Januar 2013 haben wir die NanoTite Oberfläche über den Prozess des Abstrahlens mit Kalziumphosphat weiter aufgeraut. Das Ergebnis ist die neue 3i T3 Implantatoberfläche, die nun verschiedene Rauigkeiten kombiniert:
- Eine Topografie im Submikronbereich (< 1 µ) durch die Einzelkristallauflagerung – Discrete Crystalline Deposition, DCD – von Calciumphosphat-Nanopartikeln,
- eine Topografie im Feinmikronbereich durch die doppelte Säureätzung (1–3 µ)
- und eine Topografie im Grob-Mikronbereich durch das Abstrahlen (> 10 µ).
Diese drei Rauigkeitslevel beeinflussen die Einheilung in der frühen Phase und können nach Mendes et al. und Davies et al. damit den gesamten Prozess der Osseointegration unterstützen.
Einen ganz anderen Weg geht Zimmer Dental, zumindest bei einem Implantat …
Collins: Richtig, beim Trabecular Metal, hier setzen wir auf die sogenannte Osseoinkorporation.
Darunter versteht man …
Collins: … eine Kombination aus Osseointegration und Einwachsen von Knochen in ein hoch poröses Biomaterial. Unsere Trabecular Metal Zahnimplantate besitzen ein massives, konisches Schraubendesign mit einer Oberfläche aus mäßig aufgerautem Titan, geschaffen durch Abstrahlen mit Hydroxylapatit(HA)-Partikeln, und einen mittleren Abschnitt aus hoch porösem, auf Tantal basierendem Material.
Das Material wird doch schon seit Jahren zur zementlosen Verankerung von orthopädischen Implantaten – etwa künstlichen Hüftgelenken – verwendet …
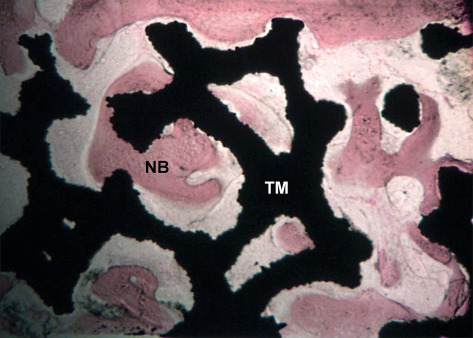
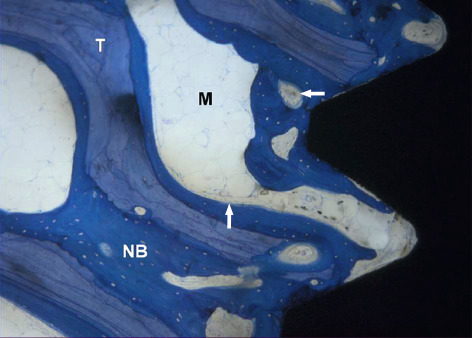
Collins: Richtig, und es hat sich mit seiner ausgedehnten Oberflächen-Mikrotextur für Knochen-Implantat-Kontakt und seiner dreidimensionalen, interkonnektierten Porosität für das Einwachsen von vaskularisiertem Knochen in der Praxis bewährt (Abb. 17), besonders bei schlechter Knochenqualität, also in Situationen, in denen eine verbesserte Sekundärstabilität notwendig ist. In einer internationalen Proof-of-Principle-Studie erreichten Trabecular Metal Zahn‧implantate bei Sofortbelastung außer Okklusion innerhalb von 48 Stunden nach Insertion und definitiver Belastung in Okklusion sieben bis 14 Tage später eine Überlebensrate von 97,3 Prozent, und nach einem Jahr in klinischer Funktion kam es zu einem Knochenverlust von 0,43 ± 0,41 mm, berechnet ab dem Tag der Insertion.
Zusätzlich zu gesunden Patienten beurteilt die Studie auch Implantatinsertionen bei Patienten mit Osteoporose, Parodontitis, dentalen Infektionen, Knochen vom Typ IV, bei Rauchern, Knirschern und bei augmentiertem Knochen. Zwei-Jahres-Zwischenergebnisse werden beim Kongress der Academy of Osseointegration im Jahr 2014 vorgestellt.
Sie bieten aber auch „normale“ Implantantoberflächen?
Collins: Wir stellen auch Implantate mit nur der MTX-Oberfläche (Abb. 16) sowie mit strategisch platzierter, thermisch konditionierter Hydroxylapatit(HA)-Beschichtung (MP-1 HA Selective Surface) her, die aus der aufgerauten MTX-Oberfläche in der zervikalen und apikalen Region und einer hoch kristallinen HA-Beschichtung (Abb. 17) besteht, die im mittleren Abschnitt des Implantatkörpers für Kontakt mit trabekulärem Knochen aufgebracht wird. Alle unsere Implantate sind für sofortige Belastung innerhalb von 48 Stunden nach Implantat‧insertion zugelassen, wenn diese bei ausgewählten Patienten akzeptabel ist.
Kommen wir zur Sekundärstabilität: Welchen Einfluss hat die Oberflächenbeschaffenheit auf den Knochenheilungsprozess?
Biehl: Mikroraue Oberflächen nehmen durch eine verstärkte Osteoblastendifferenzierung und eine Verbesserung der thrombogenen Eigenschaften Einfluss auf den Knochenheilungsprozess. Dies führt zu einer erhöhten Knochenbildungsrate und einer höheren Festigkeit der Implantat-Knochen-Verbindung. Belege dafür finden sich unter anderem in Langzeitstudien von No‧vaes et al. und Ellingsen et al.
Appert: Fakt ist: Die Oberflächenstruktur des Implantats beeinflusst die Dynamik der Knochenneubildung. Bei der Osseointegration spielen zwei Faktoren eine wichtige Rolle: die Primärstabilität, also die mechanische Stabilität, und die Sekundärstabilität, also die biologische Stabilität nach dem Knochenumbau des Implantats im Knochen. Bei herkömmlichen Oberflächen sind die Implantate wegen des Nachlassens der Gesamtstabilität zwischen Woche zwei und vier einem höheren Versagensrisiko ausgesetzt.
Und bei mikrorauen, hydrophilen Oberflächen?
Appert: Unser SLActive verkleinert das Risiko während der kritischen Einheilphase und verbessert die Implantatintegration. Da die Knochenbildung früher einsetzt, kommt es zu einer erheblich verbesserten Implantatstabilität während des Zeitraums der kritischen Stabilitätslücke zwischen Woche zwei und vier.
Ist das belegt?
Appert: Ja, in einer kürzlich veröffentlichen Studie konnten die Vorteile nachgewiesen werden, wenngleich sowohl für SLA als auch SLActive Implantate ähnliche Einheilmuster beobachtet wurden, war der Knochen-Implantat-Kontakt (BIC) bei SLActive nach 14 Tagen größer und nach 28 Tagen signifikant größer. Dieser deutlich höhere BIC-Wert führt zu einer verbesserten Vorhersagbarkeit der Behandlung und trägt dazu bei, die Gefahr eines frühen Implantatmisserfolgs zu minimieren.
Die Oberflächenbearbeitung beeinflusst viele Faktoren, die für die Osseointegration wichtig sind. Bitte nennen Sie Beispiele.
Strauß: Zum Beispiel die Retention des Blutkoagulums, die Thrombozytenaktivierung, die mechanische Verzahnung mit der Zementlinie des Knochenaufbaus. Das Zusammenspiel all dieser Wirkungen begünstigt den Knochen-zu-Implantat-Kontakt nach der Osseointegration und unterstützt den klinischen Langzeiterfolg bei vielen klinischen Indikationen.
Herr Dr. Collins, Zimmer Dental spricht von einer Osseoinkorporation, was ist das genau?
Collins: Im sogenannten Osseoinkorporationsmodell wächst vaskularisierter Knochen in die dreidimensionale poröse Struktur des Implantats ein, zusätzlich zur Osseointegration mit den Implantatoberflächen. Der Elastizitätsmodul von Trabecular Metal Material (~3 GPa) liegt näher bei dem des kortikalen (~15 GPa) und trabekulären Knochens (~0,1 GPa) als das von Titan (~110 GPa). 26 Studien untersuchen derzeit, wie diese Unterschiede in der sekundären Stabilität die langfristige Knochenreaktion beeinflussen.
Sie alle als Premiumhersteller haben den Erfolg Ihrer Implantatoberflächen-Strukturen in einer ganzen Palette von wissenschaflichen Studien nachgewiesen.
Nur wenige Hersteller dokumentieren in eigenen klinischen Studien das Verhalten des marginalen Knochens ab dem Tag der Insertion…
Holst: Das stimmt, häufig wird dieser relevante Parameter erst Monate später erhoben, etwa bei Eingliederung der definitiven Versorgung. Also nachdem der initiale Knochenumbau bereits stattgefunden hat.
Nobel Biocare dokumentiert die sogenannte Baseline aber grundsätzlich auch in den eigenen klinischen Studien.
Wie sind die Ergebnisse?
Holst: Im Allgemeinen zeigt sich, dass nach den ersten Monaten der Einheilphase das marginale Knochenniveau stabil bleibt. In einer Elfjahresstudie über Implantate mit einer externen Sechskantverbindung und TiUnite-Oberfläche, die alle unter Sofortbelastung vornehmlich im anspruchsvollen weichen Knochen gesetzt wurden, betrug der mittlere marginale Knochenumbau im ersten Jahr 1,2 mm bei Messung ab Insertion. Der marginale Knochen verblieb nach dem ersten Jahr bei einer mittleren jährlichen Veränderung von weniger als 0,05 mm über den Zeitraum von zehn Jahren nahezu stabil. Dieses liegt deutlich unter den in der Literatur akzeptierten jährlichen Umbauraten von 0,2 mm marginalen Knochenverlusts.
Die oben genannte Studie bezogt sich auf eine Flach-zu-flach-Verbindungen. Wie sieht es bei den konischen Implantatlinien aus?
Holst: Bei jüngeren Implantatgenerationen mit konischer Innenverbindung und ‧TiUnite-Oberfläche wurde in Ein- und Zweijahresstudien ein noch deutlich geringerer mittlerer marginaler Knochenumbau von nur 0,1 mm ab Insertion gemessen.
Herr Dr. Biehl, DENTSPLY Implants setzt ja primär auf konische Verbindungen …
Biehl: Wir haben ja bekanntlich weltweit erfolgreiche Systeme sowohl mit konischer als auch mit parallelwandiger Innenverbindung. Unsere prospektiven Langzeitstudien mit einem klinischen Follow-up von über fünf Jahren belegen ein stabiles Knochenniveau für beide Oberflächen unseres Hauses, d. h. sowohl für die OsseoSpeed Oberfläche auf unserem Astra Tech Implantat System als auch für die Friadent plus Oberfläche auf Ankylos und Xive. Das Knochenniveau liegt dabei deutlich über dem, was in der wissenschaftlichen Literatur üblicherweise als „Standard“ bei der dentalen Implantatversorgung angesehen wird.
Welcher Knochenabbau gilt als akzeptabel?
Appert: Allgemein bekannt sind Knochenverluste von bis zu 1 mm im ersten Jahr (bone remodeling). In den folgenden Jahren gilt ein Knochenverlust von bis zu 0,2 mm als klinisch unkritisch.
Um Knochenabbau über einen längeren Zeitraum exakt und standardisiert zu messen, sind prospektive Studien notwendig. Für die Straumann TL SLA Implantate wurden drei dieser Langzeitstudien publiziert, in denen auch das Knochenniveau bestimmt wurde.
In der Studie von Fischer et al. 2012 wurde ein durchschnittlicher Knochenverlust nach zehn Jahren von 1 mm bei 102 Implantaten bestimmt. Dieser Wert liegt somit deutlich unter dem kritischen Wert. Viel aussagekräftiger als Durchschnittswerte ist die Bestimmung der Häufigkeitsverteilung des Knochenverlusts. Buser et al. 2012 bestimmten an 505 Implantaten den Anteil der Implantate, die mehr als 0,2 mm Knochenverlust pro Jahr über zehn Jahre hinweg aufwiesen. Nur 22 Implantate, also 4,4 Prozent, zeigten einen höheren Wert, wobei nur neun Implantate als klinisch auffällig bewertet wurden. Die übrigen 13 Implantate zeigten keinerlei Zeichen von periimplantären Infektionen. In der Studie von Roccuzzo et al. 2013 wurde der Knochenverlust von parodontal gesunden mit dem von parodontal beeinträchtigten Patienten verglichen. In der Gruppe der parodontal gesunden Patienten wurde bei keinem Implantat ein Knochenverlust von mehr als 3 mm während der zehn Jahre bestimmt. Bei den parodontal beeinträchtigten Personen wiesen etwa zehn Prozent einen Knochenverlust von mehr als 3 mm auf.
Aufgrund solcher Langzeitstudien können wir davon ausgehen, dass nur ein sehr geringer Anteil an Patienten einen klinisch relevanten Knochenverlust am Implantat erleidet und selbst bei den parodontal beeinträchtigten Patienten liegt dieser Wert nicht über zehn Prozent.
Welche Rolle spielt dabei das Implantatdesign?
Große Holthaus: Eine erhebliche, der Knochenabbau kann nicht nur mit der Oberflächenbehandlung in Zusammenhang gebracht werden. Er ist unter anderem abhängig von der Art der Belastung sowie der prothetischen Konstruktion. Unter Berücksichtigung bestimmter statischer Gesetzmäßigkeiten erfolgt bei den BEGO Semados Implantaten kein bis zu einem moderaten Knochenabbau. Vorteilhaft hierbei sind die bei unseren Implantaten verwendeten Mikrorillen/Mikrogewinde zur Vergrößerung der Implantatoberfläche. Diese sorgen für eine erhöhte Knochenbedeckungsrate im entscheidenden krestalen Knochen.
Betrifft das nicht vor allem die Primärstabilität?
Große Holthaus: Nicht nur. Die Primärstabilität des Implantats wird zum einen durch die Art und Technik der chirurgischen Aufbereitung der Kavität eingeleitet und zum anderen durch die Implantatform und das Gewindedesign. Wir verwenden seit vielen Jahren eine gestrahlt-geätzte Oberfläche, TiPurePlus, mit einer mittleren Flächenrauheit von ca. 1,6 µm. Und: Eine homogen verteilte Flächenrauigkeit der Implantatoberfläche von 1 bis 2 µ ist vorteilhaft für eine gute Osseointegration. Das wurde bereits in unterschiedlichen Publikationen beschrieben.
Gibt es weitere „Erfolgsgaranten“?
Holst: Neben der Qualität des Implantats und der Oberfläche sind ein engmaschiges Recallprogramm und eine gute Compliance des Patienten ein Schlüsselfaktor für stabile Langzeitergebnisse. Das zeigt eine prospektive Zehnjahresstudie mit teilbezahnten Patienten, die TiUnite Implantate erhielten, die ein- oder zweizeitig gesetzt wurden. Es wurden eine kumulative Überlebensrate von 99,2 % und ein mittlerer marginaler Knochenumbau ab Tag der Belastung von 0,7 mm über den gesamten Zeitraum von zehn Jahren gemessen.
Strauss: Ich halte Platform-Switching für einen weiteren wichten Parameter. Bei sofort belasteten BIOMET 3i Implantaten mit integriertem Platform-Switching wie Osseotite Certain Prevail , NanoTite Certain Prevail oder 3i T3 Implant liegt der krestale Knochenabbau im günstigsten Fall bei nur 0,39 mm nach einem Jahr.
Collins: Die Ursachen von krestalem Knochenverlust sind ja oft sehr komplex. Zu den zahlreichen in der Fachliteratur berichteten Risikofaktoren für periimplantären krestalen Knochenverlust gehören unter anderem Operationstrauma, Komorbiditäten wie etwa Parodontitis, Periimplantitis und Osteoporose, zu niedrige Östrogenwerte, Rauchen, Bruxismus, okklusale Überlastung. Ormianer und Palti berichteten retrospektiv über die Ergebnisse von 172 Implantaten mit MTX-Oberflächen nach zehn Jahren in Funktion. Die meisten Implantate hatten keinen Knochenverlust. Bei den restlichen 57 Implantaten reichte der Knochenverlust von 0,5 mm oder weniger bis zu 1,5 mm oder weniger, 2,5 mm oder weniger und 3,5 mm oder weniger. Die meisten Implantate mit Knochenverlust fanden sich bei Patienten mit einer früheren Parodontalerkrankung und bei Frauen, ungeachtet ihres Parodontalstatus.
Was bewirken Mikrorillen?
Große Holthaus: Mikrorillen und Mikrogewinde dienen zur Vergrößerung der Implantatoberfläche. Sie sorgen für eine erhöhte Knochenbedeckungsrate (KBR) im entscheidenden krestalen Knochen.
Holst: Mikrorillen werden seit 2005 auf den Gewinden der meisten unserer Implantate angebracht, da in präklinischen In-vivo-Untersuchungen gezeigt werden konnte, dass eine 110 Mikrometer messende Mikrorille statistisch signifikant zu einer verbesserten Osseointegration im Vergleich zu Implantaten ohne Rille oder mit einer anders dimensionierten/positionierten Rille führte. Der Knochen wächst vor allem entlang der Rille, was zusammen mit dem osteokonduktiven Effekt der TiUnite-Oberfläche zu einer schnelleren Einheilung führt. Der positive Effekt bestätigte sich auch im „Split-Mouth-Design“ mit ähnlichen Implantattypen, mit und ohne Mikrorille.
Beide Implantate zeigten hervorragende Ergebnisse, wobei Implantate mit Mikrorille signifikant weniger marginalen Knochenumbau nach mehr als einem Jahr aufwiesen.
Mikrorillen können aber auch zu ausgesprochen negativen Effekten führen, bis hin zum Implantatverlust …
Appert: Das ist richtig, falls sie freiliegen, können sie von Bakterien besiedelt werden. Eine Entfernung der bakteriellen Plaque ist kaum möglich, und das führt schließlich zu einem katastrophalen Implantatverlust. Bei einer guten Oberfläche im Hartgewebeteil sind unserer Meinung nach Mikrorillen von sekundärer Bedeutung.
Zurück zu den maschinierten Implantatschultern …
Große Holthaus: Eine maschinierte Implantatschulter ermöglicht die reizfreie Anlagerung der Gingiva an die Implantatoberfläche und zudem die Reinigung bei unebenem Knochenniveau.
Holst: TiUnite zeigte im Vergleich zu maschinierten Schultern in humanhistologischen Studien eine verbesserte Anlagerung des Bindegewebes, und es konnte auch eine für Implantate ungewöhnliche funktionelle Ausrichtung von Kollagenfasern an der TiUnite-Oberfläche nachgewiesen werden. TiUnite-beschichtete Schultern zeigten im Vergleich zu maschinierten Oberflächen in einer dreijährigen Studie im randomisierten, kontrollierten „Split-Mouth-Design“ bei parodontal vorgeschädigten Patienten keine signifikanten Nachteile bezüglich mikrobiologischer und biochemischer Parameter.
Mit anderen Worten: Mikrorillen und moderat raue Oberflächen dienen der Osseointegration, bergen aber die Gefahr der Biofilmanlagerung, wenn sie freiliegen. Was ist die Lösung?
Holst: Nobel Biocare bietet neben Schultern mit TiUnite-Oberfläche auch voll- und teilmaschinierte Schultern an, so dass je nach Gegebenheiten am Patienten und avisierter Insertionstiefe dem Behandler verschiedene Behandlungsoptionen zur Verfügung stehen, die auf die individuellen Bedürfnisse des Patienten angepasst werden können.
Daneben gibt es ein Implantat mit einer drei Millimeter hohen, maschinierten Schulter, die für Stegprothesen und diverse Deckprothesenlösungen entwickelt wurde.
Biehl: Auch im Portfolio der DENTSPLY Implants sind beide Implantatvarianten verfügbar, also mit Mikrorillen und maschinierten Schultern. Beide zeigen eine sehr gute klinische Performanz. Die Oberfläche bestimmt das frühe Stadium des Heilungsprozesses. Für den Erhalt des Gewebes sind andere Designeigenschaften, wie beispielsweise das Gewindedesign oder die Implantat-Abutment-Verbindung, maßgeblich (Abb. 10a-d, 11a-b)).
Appert: Maschinierte Implantatschultern neigen zu sehr wenig Plaqueanlagerung und stören somit die Weichgewebeanlagerung nicht. Das Weichgewebe an Implantatschultern ist aber anders strukturiert als am lebenden Zahn mit paradontalem Ligament und Sharpey-Fasern. Ich könnte mir aber gut vorstellen, dass sich Oberflächen entwickeln lassen, die zu einem zahnähnlichen Abschluss des Weichgewebes führen könnten. Ziel müsste es sein, die Gefahr von Periimplantitis weiter zu reduzieren. Diese Entwicklungen sind aber noch im Forschungsstadium.
Collins: Die Trabecular Metal und Tapered Screw-Vent Zahn-implantate sind mit zervikalen Mikrorillen und MTX-Oberflächenmikrotextur erhältlich, die sich entweder bis zum koronalen Rand des Implantats erstrecken oder unterhalb einer minimalen, etwa 0,5 bis 1,0 mm maschinierten (gedrehten) Oberfläche enden, die sich unmittelbar unter dem koronalen Rand befindet.
Die radialen Mikrorillen sind um die zervikale Region des Implantats maschinengefräst. Anders als zervikale Mikrogewinde besitzen radiale Mikrorillen eine gewellte Geometrie.
Die vom Implantat während okklusaler Belastung auf den Knochen übertragenen Kräfte können grob eingeteilt werden in vertikale (komprimierende) oder horizontale (scherende) Kräfte.
- Der primäre Zweck unserer zervikalen Mikrorillen besteht darin, die Kraftübertragung vom koronalen Anteil des Implantats auf die krestale Knochenregion zu reduzieren und damit zur Erhaltung der marginalen Knochenhöhe beizutragen.
- Der sekundäre Zweck unserer Mikrorillen ist, das Einwachsen von Knochen in die Rillen zu erleichtern und somit eine Versiegelung gegen Bakterien und nach unten gerichtetes Epithelwachstum zu schaffen. In einer Reihe von zellulären Studien in vitro und in vivo berichteten Chehroudi et al. 35–37, dass horizontale Mikrorillen wirksam bei der Verhinderung von nach unten gerichtetem Epithelwachstum sind und dass sich Fibroblastenzellen in horizontale Mikrorillen mit einer Tiefe von ≥ 10 µm einlagerten und dieses Epithelwachstum blockierten.
Frau Strauß, was halten Sie von maschinierten Implantatschultern?
Strauß: Obwohl diese Eigenschaften an der Implantatschulter den krestalen Knochenabbau beeinflussen könnten, glauben wir bei BIOMET 3i, dass es keinen stichhaltigen wissenschaft‧lichen Beweis gibt, der diese Annahme stützt. Daher verfügen unsere Implantatschultern derzeit nicht über diese Eigenschaften. Dennoch haben unsere moderneren Implantate wie Certain Prevail Implantate, die „Osseotite 2“ parallelwandigen Implantate und die 3i T3 Implantate die mikroraue Osseotite Oberfläche am oberen Teil der Implantatschultern. Die bestdokumentierten Implantateigenschaften, die den krestalen Knochenerhalt unterstützen, sind noch immer das Platform-Switching und eine versiegelte Implantat-Abutment-Verbindung. Die Versiegelung und die BIOMET 3i Certain Verbindung sowie die Gold-Tite Schraube können den Erhalt des krestalen Knochens positiv beeinflussen.
„Alle Jahre wieder“ steht die Materialfrage an: Macht eine weiße Oberflächenbeschichtung der grauen Titanimplantate Sinn?
Holst: Graue Oberflächen machen sich erst bei starkem marginalen Knochenverlust bemerkbar, dessen Ursache generell untersucht werden muss. Bei entsprechender Behandlungsplanung und Ausführung und Verwendung geeigneter Komponenten für eine spezifische Indikation wird ein Implantat nicht sichtbar. Die entsprechende Distanz zwischen Implantatschulter und klinischer Krone kann hervorragend mit einem individuellen Abutment überbrückt werden. Durch zahlreiche In-vitro- und In-vivo-Ergebnisse wissen wir, dass beispielsweise Zirkonabutments ebenso gut funktionieren wie Titanabutments.
Appert: Zunächst einmal: Titanimplantate sind in den wenigsten Fällen ein ästhetisches Problem. Im Einsatz zusammen mit vollkeramischen Abutments lassen sich in den meisten Fällen perfekte Rekonstruktionen erzielen, ohne dabei Kompromisse bei den Festigkeiten zu machen. In Ausnahmefällen, z. B. bei Patienten mit dünnem parodontalem Biotyp, können Titanimplantate in der ästhetischen Zone durchscheinen.
Biehl: Implantate von DENTSPLY Implants erhalten nachweislich Hart- und Weichgewebe, insofern führt die graue Farbe der Implantate in der Mehrzahl der Fälle nicht zu ästhetischen Problemen. Hinzu kommt, dass im Portfolio der DENTSPLY Implants Abutments aus alternativen Werkstoffen oder von anderer Farbe verfügbar sind, wie zum Beispiel aus Zirkondioxid oder goldfarbenem Titan. Mit ihnen lassen sich selbst Situationen höchster ästhetischer Ansprüche oder besonders dünner Gingiva hervorragend meistern.
Grosse Holthaus: Idealerweise ist die implantologische/prothetische Versorgung so gut, dass die graue Erscheinung des Titans kein Problem darstellt. Helle, weißliche Biokeramiken wie Zirkonoxid könnten eine Alternative sein. Diese Materialien erreichen jedoch meist keine so gute Osseointegration wie das bewährte Titan, das vielseitig oberflächentechnisch modifizierbar ist. Sie sind wegen ihrer typischen keramischen Materialeigenschaften – etwa Sprödigkeit – schwierig oder kaum mechanisch an der Implantatoberfläche bearbeitbar. Ebenso ist ihre mechanische Festigkeit im Vergleich zu Titan in vielen entscheidenden Bereichen deutlich geringer. Weiße Beschichtungen wie Calziumphosphatkeramiken – Hy‧dro‧xyl‧apatit oder ß-Tricalziumphosphat – bieten nur dann eine Alternative, wenn die Beschichtung eine ausreichende Adhä‧sion zum Implantat aufweist und ggf. die Beschichtung im Einklang mit dem neuen Knochenaufbau resorbiert wird.
Strauss: Die graue Farbe kann dann zum Problem werden, wenn Knochen und Gingiva zurückgehen. Mit einer Oberflächenbehandlung auf der gesamten Implantatlänge, mit integriertem Platform-Switching und einer versiegelten Implantat-Abutment-Verbindung sowie der Gold-Tite Schraube können die Implantate von BIOMET 3i nachhaltige ästhetische Ergebnisse erzielen. Wir erforschen kontinuierlich neue Werkstoffe und entwickeln Implantatdesigns, um nachhaltige ästhetische Ergebnisse zu unterstützen.
Fakt ist, viele Patienten wünschen eine metallfreie Versorgung. Welche Titan-Alternativen bieten sich an?
Holst: Unserer Ansicht nach gibt es keine ausreichende qualitative klinische Evidenz dafür, dass weiße Implantate wie ZrO2-Keramikimplantate den Titanimplantaten gleichwertig oder gar überlegen sind. So existiert keine valide klinische Langzeitstudie, also ≥ 5 Jahre, die einen erfolgreichen Einsatz dieser Implantate belegt. In einer von Nobel Biocare initiierten Fünfjahresuntersuchung von ZrO2-Keramikimplantaten zeigte sich z. B. ein Rückgang der klinischen Überlebensrate erst nach drei Jahren. Dieser negative Trend wurde auch in den folgenden zwei Jahren beobachtet, was letztlich zu der Entscheidung führte, ein entsprechendes Produkt nicht auf den Markt zu bringen.
Also halten Sie sich zurück?
Holst: Hier sehen wir im Markt leider viele Ansätze, bei denen eine entsprechende klinische Sicherheit für den Patienten nicht dokumentiert ist. Es sind weitere intensive Langzeituntersuchungen notwendig, um verantwortungsvoll diese „weißen Implantate“ auf den Markt zu bringen und einzusetzen. Eine aktuelle Vergleichsstudie von 2013 belegt beispielsweise den statistisch signifikant besseren marginalen Knochenerhalt der Titaimplantate im Vergleich zu den Keramikimplantaten. Da für Nobel Biocare die Sicherheit und Zufriedenheit des Patienten an erster Stelle steht, empfehlen wir die Verwendung wissenschaftlich bewiesener Systeme und Produkte, werden aber zukünftig intensiv weiter an Innovationen arbeiten.
Straumann hat auf dem EAO-Kongress in Dublin ein klinisch validiertes Vollkeramikimplantat vorgestellt …
Appert: Richtig, denn zum Teil wünschen Patienten, metallfrei behandelt zu werden. Mit weißen Oberflächenbeschichtungen kommt man da nicht weiter. Nur Vollkeramikimplantate können dem Anspruch der Metallfreiheit genügen. Bisher waren aber nur Keramikimplantate von kleineren Firmen im Markt verfügbar, die nur unzureichend mit klinischen Daten dokumentiert sind (Abb. 6 bis 9). Mit dem Ceramic Implant Monotype (CIM) bieten wir eine sichere Alternative zu Titanimplantaten in ästhetisch anspruchsvollen Situationen, aber auch, wenn metallfreie Restaurationen gewünscht werden.
Literaturverzeichnis